自由電子
 電気・熱伝導性、光反射率、機械物性
電気・熱伝導性、光反射率、機械物性
<金属結合>
 電気・熱伝導性、光反射率、機械物性
電気・熱伝導性、光反射率、機械物性
<共有結合とイオン結合>
共有結合:電子の共有による結合
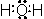
イオン結合:静電的な引力による結合
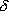 + -
Cl
+ -
Cl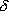 -
note) 多くの結合:共有性+イオン性
(cf. 3.4 Paulingの電気陰性度)
-
note) 多くの結合:共有性+イオン性
(cf. 3.4 Paulingの電気陰性度)
| 指標 1 |  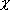 > 1.7 : イオン性結合 > 1.7 : イオン性結合 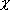 < 1.7 : 共有結合性 < 1.7 : 共有結合性
| |
| 指標 2 | イオン結合度 = 1 - exp[- 0.25
( 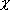 )2] )2]
|
4.1.1 最密充填構造
4.1.2 非最密充填構造
<配位数>
| 最密充填 | 12 |
| 体心立方 | 8 or 14 (6 個は距離が少し[約15%]遠い) |
| 単純立方 | 6 |
| ダイアモンド構造 | 4 |
| hcp | Be, Cd, Co, Mg, Ti, Zn |
| fcc | Ag, Al, Au, Ca, Cu, Ni, Pb, Pt |
| bcc | Ba, Cr, Fe, W, アルカリ金属 |
| (cubic-P) | Po |
<転位>
・高温 : bcc など非最密 / 高圧 : hcp など最密充填
ex.) Fe
| ~ 906 ℃ |  -Fe (bcc) -Fe (bcc)
|
| 906 ~ 1401 ℃ | 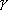 -Fe (fcc) -Fe (fcc)
|
| 1401 ~ 1530 ℃ (m.p.) |  -Fe (bcc) -Fe (bcc)
|
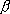 -Fe(hcp)
... 高圧で生成
-Fe(hcp)
... 高圧で生成 ,
,
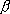 ,
, 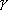 ,
... とラベル
,
... とラベル
ex.) Sn
| 常温 | 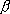 -Sn -Sn(白色スズ) | ダイアモンド変形構造 7.31g cm-3 |
| < 14.2 ℃ (slow) |  -Sn -Sn(灰色スズ) | ダイアモンド構造 5.75 g cm-3 |
4.3.1 半径比則
一般に 陰イオン > 陽イオン
陰イオン(最密)充填構造の間隙に陽イオンが入る(逆もある)
<配位数> 陽イオンが対陰イオンで配位される数
<半径比> 陽イオンの半径 r + と陰イオンの半径 r - の比 (r + / r -)
<半径比則> 半径比で好まれる構造(配位数)が異なること
 半径比 0.611
半径比 0.611
 正八面体6配位構造
正八面体6配位構造
4.3.2 代表的な結晶構造
MX 型 (陽イオン : 陰イオン = 1 : 1)
| 結晶構造 | 配位数 | 基本骨格 | 代表例 |
| 1) 塩化セシウム (CsCl) 型 | 8 | bcc 各層に交互に M と X | CsBr, TlCl, NH4Cl |
| 2) 岩塩 (NaCl) 型 | 6 | X ccp の八面体間隙に M | AgF, MgO, CaS |
| 3) ヒ化ニッケル (NiAs) 型 | 6 | X hcp の八面体間隙に M | FeS, NiS |
| 4) 閃亜鉛鉱型 (ZnS) | 4 | X ccp の四面体間隙の半分に M | BeS, GaAs |
| 5) ウルツ鉱型 (ZnS) | 4 | X hcp の四面体間隙の半分に M | BeO, SiC, ZnO |
MX2 型 (陽イオン : 陰イオン = 1 : 2)
| 結晶構造 | M 配位数 | X 配位数 | 基本骨格 | 代表例 |
| 1) 蛍石 (CaF2) 型 | 8 | 4 | M ccp の四面体間隙に X | SrF2, BaCl2 |
| 1') 逆蛍石型 | 4 | 8 | X ccp の四面体間隙に M | Li2Te, Na2O |
| 2) ルチル (TiO2) 型 | 6 | 3 | X hcp の八面体間隙の半分に M | SnO2, MgF2 |