 エネルギー同じ (s, p, d, ... 軌道が縮退)
エネルギー同じ (s, p, d, ... 軌道が縮退)
<Bohr軌道>
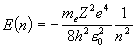
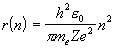
<水素原子類似軌道>
 エネルギー同じ (s, p, d, ... 軌道が縮退)
エネルギー同じ (s, p, d, ... 軌道が縮退)
<軌道節面>
ex.)
軌道 角度方向節 動径方向節 合計 1s 0 0 0 2s 0 1 1 2p 1 0 1 3s 0 2 2 3p 1 1 2 3d 2 0 2 cf.) 分子軌道でも一般に節の多い軌道ほどエネルギーが高い
節の数古典的周波数, 1/(電子の運動周期)
E = h
<遮蔽>
ex.) Li 原子:電子配置1s22s1 1s 電子の電荷(-)で遮蔽され小さくなる:有効核電荷
(Zeff, Z*)
1s 電子の電荷(-)で遮蔽され小さくなる:有効核電荷
(Zeff, Z*)
<Slaterの規則>
 遮蔽 1
遮蔽 1
<貫入>
 [2p と比較して] 2s 軌道は 1s の内側に貫入している
[2p と比較して] 2s 軌道は 1s の内側に貫入している [ 〃 ] 1s の遮蔽をうけにくく有効な核電荷が大きい
[ 〃 ] 1s の遮蔽をうけにくく有効な核電荷が大きい [ 〃 ] エネルギーが低い
[ 〃 ] エネルギーが低い
 第4周期 4s2 の後に第1遷移金属周期
第4周期 4s2 の後に第1遷移金属周期
 構成原理
構成原理2.2.1 原子価軌道
 原子価軌道
原子価軌道2.2.2 原子価軌道の周期律
・周期律表( ) ...
原子価軌道エネルギー(
) ...
原子価軌道エネルギー(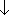 ),
原子価軌道の大きさ(
),
原子価軌道の大きさ(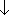 )
)
| Z | 3 (Li) | 4 (Be) | 5 (B) | (真の核電荷) |
| Z*2s (完全遮蔽) | 1 | 1 | 1 | 自分以外の電子による遮蔽が完全と仮定した場合 |
| Z*2s (Slater) | 1.30 | 1.95 | 2.60 | 実際に近い値 (Slater) |
 不完全な遮蔽の蓄積
不完全な遮蔽の蓄積
・周期律表( ) ...
原子価軌道エネルギー(
) ...
原子価軌道エネルギー( ),
原子価軌道の大きさ(
),
原子価軌道の大きさ(
 )
)
Z* の増大の効果 ≦ 主量子数増大の効果
・周期律表( ) ...
基本は同上 [エネルギー(
) ...
基本は同上 [エネルギー(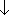 ),
大きさ(
),
大きさ(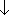 )]
)]
遷移周期中盤:性質類似 (cf. 8-10 族は 旧 VIII 族)
遷移周期後半:(n-1)d は内殻的(不完全遮蔽の蓄積) ...
化学的に安定
 11 族:
(n-1)d10 ns1,
12 族:(n-1)d10 ns2 ...
1, 2族に類似
11 族:
(n-1)d10 ns1,
12 族:(n-1)d10 ns2 ...
1, 2族に類似
特に第6周期 (第3遷移系列):(n-2)f
軌道の不完全遮蔽も加わる
 Pt, Au, Hg 安定
Pt, Au, Hg 安定
<不活性電子対効果>
周期律表で遷移金属に後続する典型元素は、 しばしば価電子数で予想されるより2小さい酸化数をとること。 ns 軌道の電子対が不活性であると解釈されるためこのように 呼ばれる。
ex.) SnII(SnCl2), PbII, TlI, InI[解釈]
遷移周期 d 軌道の不完全遮蔽蓄積は後続典型元素に影響[資料2.11]ns[貫入している]
(npに比べて) (n-1)d の遮蔽を受けにくい
内殻的・不活性
・第6周期:さらに (n-2)f の不完全遮蔽で特に不活性
・13, 14族で顕著
16-17族ではnp自信の不完全遮蔽で顕著でなくなる