(c) 2000 by A. Miyoshi, Univ. Tokyo
All rights reserved.
[Top]
問題:
[1-1]
[1-2]
[1-3]
[2]
[3]
2000物理化学及び演習II - 問題1-1
[演習問題 1-1]
もりうち機構の反応速度定数 (Na + Cl, Na + Cl2)
2つの反応、
Na + Cl 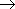 NaCl
NaCl
(1)
Na + Cl2 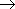 NaCl + Cl
NaCl + Cl
(2)
は「もりうち機構」で進行する。その概要を反応 (1)
の場合について下図に示す。
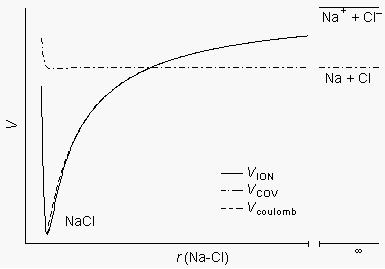
共有結合性ポテンシャル (VCOV) 上で Na と Cl
を近づけると、イオン結合性ポテンシャル (VION)
との交差点から先では VION の方が安定であるために、
ここからは VION 上を近づいていく。
交差点では Na が Cl に電子の「もり」を撃って Na+
と Cl- になり、静電力によって Cl-
を引き寄せることから「もりうち機構」と呼ばれる。
Na と Cl がこの交差点以下の距離に近づけば反応がおこる。
単純なモデルでは、VCOV は一定、すなわち、
と考えてよく、VION はクーロン引力ポテンシャル
(VCOULOMB) で近似してよい。
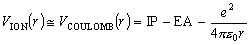
(4)
ここで IP は Na 原子のイオン化ポテンシャル (Na を Na+
+ e にするために必要なエネルギー)、EA は Cl 原子の電子親和力
(Cl + e が Cl- になって安定化するエネルギー)
である。 0
は真空の誘電率、e は電子の電荷である。
0
は真空の誘電率、e は電子の電荷である。
[問題 1-1(a)]
イオン結合性ポテンシャルと共有結合性ポテンシャルの交差点における距離
rc の式を書け。また、IP(Na) = 5.14 eV,
EA(Cl) = 3.61 eV, EA(Cl2) = 2.54 eV を用いて、反応 (1) および
(2) の場合の rc の値を求めよ。
*(注) "eV" (エレクトロンボルト/電子ボルト) は電子1個を 1 V
の電位差に逆らって移動するのに必要なエネルギーである
(V = J C-1 である)。
(1) の反応の速度は、Na と Cl が距離 rc
以下に近づくような衝突が起こる頻度である。今、Na と Cl
の相対並進運動を考えると、反応性の衝突が起こる頻度 (反応速度)
は、反応断面積、
 =
=
 rc2
rc2
(5)
を持つ Na 原子が、相対速度 v
で単位時間あたりに掃引する体積中にある Cl 原子の数である。
R (反応速度) = (単位時間の掃引体積)
 (Cl 濃度)
(Cl 濃度)
(6)
反応速度定数 k は、R を Cl 濃度で割ったものであるから、
である。絶対温度 T における平均相対並進速度は、
マクスウェル-ボルツマン速度分布から、
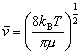
(8)
となる。ここで、kB はボルツマン定数、
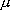 は2個の粒子の換算質量、
は2個の粒子の換算質量、
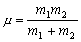 (m1, m2: 各粒子の質量)
(m1, m2: 各粒子の質量)
(9)
である。
[問題 1-1(b)]
(7) 式の反応速度定数を、rc,
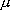 ,
T から評価する式を書け。また (1), (2) の反応の、反応断面積
[単位:
,
T から評価する式を書け。また (1), (2) の反応の、反応断面積
[単位: 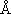 2]、298 K
における反応速度定数 [単位: cm3 molecule-1
s-1 (cm3 s-1)] を計算せよ。原子の質量は、
m (Na) = 23.0 amu, m (Cl) = 35.0 amu である。
(2) の反応速度定数の実測値 (298 K)、6.7
2]、298 K
における反応速度定数 [単位: cm3 molecule-1
s-1 (cm3 s-1)] を計算せよ。原子の質量は、
m (Na) = 23.0 amu, m (Cl) = 35.0 amu である。
(2) の反応速度定数の実測値 (298 K)、6.7  10-10 cm3 s-1
と計算値を比較せよ。
10-10 cm3 s-1
と計算値を比較せよ。
*(注) 'amu' (atomic mass unit / 原子質量単位) は 12C
の原子核の質量の 1/12 と定義される。アボガドロ数 NA
は、1モルの 12C の質量が正確に 12 g
となるように定義されている。
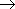 NaCl
NaCl
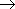 NaCl + Cl
NaCl + Cl
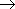 NaCl
NaCl
 NaCl + Cl
NaCl + Cl

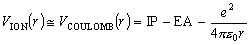
 0
は真空の誘電率、e は電子の電荷である。
0
は真空の誘電率、e は電子の電荷である。
 =
=
 rc2
rc2
 (Cl 濃度)
(Cl 濃度)
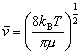
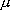 は2個の粒子の換算質量、
は2個の粒子の換算質量、
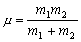 (m1, m2: 各粒子の質量)
(m1, m2: 各粒子の質量)
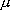 ,
T から評価する式を書け。また (1), (2) の反応の、反応断面積
[単位:
,
T から評価する式を書け。また (1), (2) の反応の、反応断面積
[単位: 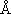 2]、298 K
における反応速度定数 [単位: cm3 molecule-1
s-1 (cm3 s-1)] を計算せよ。原子の質量は、
m (Na) = 23.0 amu, m (Cl) = 35.0 amu である。
(2) の反応速度定数の実測値 (298 K)、6.7
2]、298 K
における反応速度定数 [単位: cm3 molecule-1
s-1 (cm3 s-1)] を計算せよ。原子の質量は、
m (Na) = 23.0 amu, m (Cl) = 35.0 amu である。
(2) の反応速度定数の実測値 (298 K)、6.7  10-10 cm3 s-1
と計算値を比較せよ。
10-10 cm3 s-1
と計算値を比較せよ。