 = 5~20 dm3 mol-1 cm-1) の UV
吸収スペクトルを測定したい。測定セルの光路長は 1 cm であり、
分光光度計の雑音などから透過率 90% 以上や 5% 以下の吸収は
精度よく測定できない。測定試料はどの程度の濃度に調整すればよいか?
= 5~20 dm3 mol-1 cm-1) の UV
吸収スペクトルを測定したい。測定セルの光路長は 1 cm であり、
分光光度計の雑音などから透過率 90% 以上や 5% 以下の吸収は
精度よく測定できない。測定試料はどの程度の濃度に調整すればよいか?講義中に示した演習問題
問題 1.1
あるカルボニル化合物 (推定吸光係数  = 5~20 dm3 mol-1 cm-1) の UV
吸収スペクトルを測定したい。測定セルの光路長は 1 cm であり、
分光光度計の雑音などから透過率 90% 以上や 5% 以下の吸収は
精度よく測定できない。測定試料はどの程度の濃度に調整すればよいか?
= 5~20 dm3 mol-1 cm-1) の UV
吸収スペクトルを測定したい。測定セルの光路長は 1 cm であり、
分光光度計の雑音などから透過率 90% 以上や 5% 以下の吸収は
精度よく測定できない。測定試料はどの程度の濃度に調整すればよいか?
問題 1.2 35Cl2 を 330 nm で光分解した。分解直後の Cl 原子の飛行速度を求めよ。Cl-Cl 結合エネルギーは 242.6 kJ mol-1である。
問題 1.3 凝縮相でのスペクトル線幅は、周囲の分子との相互作用による 不均一幅が支配的である。液相と単結晶固相中でのスペクトル線幅はどちら が細いか?
例題 1.1
1) NH3 の190 nm の吸収線幅 140 cm-1 (HWHM)
から、励起状態の寿命を推定せよ
1 / (2
 140
140  100
100  c0)
= 3.8
c0)
= 3.8  10-14 s = 38 fs (フェムト秒)
10-14 s = 38 fs (フェムト秒)
2) 298 K において H 原子の Lyman- 線 (121.534 nm)
のドップラー幅 (HWHM) は?
線 (121.534 nm)
のドップラー幅 (HWHM) は?
(1 / 121.534  10-9)
10-9)
 [(2k
[(2k  298
298
 ln2) / (1.0087
ln2) / (1.0087  mu)]1/2 = 1.52
mu)]1/2 = 1.52  1010 s-1 (15.2 GHz) = 0.506 cm-1
1010 s-1 (15.2 GHz) = 0.506 cm-1
問題 1.4
大気中 (298 K, 1 atm) の CO 分子は 7.2  109 s-1 の頻度で空気中分子 (N2,
O2, etc.) と衝突する。これから衝突幅を見積り、
154.4 nm の電子遷移と 4.67
109 s-1 の頻度で空気中分子 (N2,
O2, etc.) と衝突する。これから衝突幅を見積り、
154.4 nm の電子遷移と 4.67 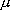 m の振動遷移について、
ドップラー幅と比較せよ。
m の振動遷移について、
ドップラー幅と比較せよ。
例題 2.1
H35Cl の赤外吸収波数 2885.98 cm-1 から
D35Cl (2H35Cl)
の赤外吸収波数を推定せよ。
kf は核質量に依存しない. 波数比は
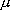 -1/2 の比 [(2.4)式].
-1/2 の比 [(2.4)式].
D35Clの赤外吸収波数 = 2885.98  (
(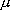 DCl /
DCl /
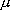 HCl)-1/2 = 2070
cm-1.
HCl)-1/2 = 2070
cm-1.
(実測値 2091 cm-1 との差は非調和性による)
問題 2.1 H37Cl, D37Cl の赤外吸収波数を推定せよ。
問題 2.2
調和振動子の  = 1,
= 1,
 = 3 の波動関数を図示し、
= 3 の波動関数を図示し、
 = 3
= 3 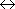 1
の遷移が禁制であることを説明せよ。
1
の遷移が禁制であることを説明せよ。
問題 2.3 N2 分子の 1) 双極子モーメント, 2) 分極率 が分子振動座標 x にどのように依存するかを示し、 赤外遷移・ラマン遷移が活性かどうかを判定せよ。
例題 3.1
12C16O の遠赤外吸収スペクトルから
結合距離 r を求めよ
J = 4 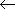 3 遷移 (15.38 cm-1)
から B = 1.9225 cm-1,
3 遷移 (15.38 cm-1)
から B = 1.9225 cm-1,
J = 10 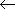 9 (38.41 cm-1) から
B = 1.9205 cm-1 [(3.10)式].
9 (38.41 cm-1) から
B = 1.9205 cm-1 [(3.10)式].
I = 8.7686, 8.7777 amu 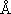 2
[(3.4b)式].
2
[(3.4b)式].
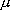 = 6.8562 amu [(2.3)式]
を用いて, r = 1.1309, 1.1315
= 6.8562 amu [(2.3)式]
を用いて, r = 1.1309, 1.1315 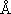 [(3.1)式]
[(3.1)式]
1 amu (原子質量単位) = 1  10-3 / NA [kg]
10-3 / NA [kg]
m(C) = 12 amu, m(O) = 15.9949 amu; 1
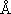 = 10-10 m
= 10-10 m
J 大で r 大となるのは、遠心歪のため
問題 3.1
オリオン星雲から観測される 86243.28 MHz のマイクロ波は
振動励起状態 ( = 1) の
28Si16O の J = 2
= 1) の
28Si16O の J = 2 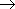 1 遷移である。これからこの状態の SiO の核間距離を求めよ。
1 遷移である。これからこの状態の SiO の核間距離を求めよ。
問題 3.2
H2 分子の核間距離は 0.742 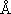 である。これから H2 (1H1H) および
D2 (2H2H)
分子の回転ラマンスペクトルの間隔を予想せよ。
である。これから H2 (1H1H) および
D2 (2H2H)
分子の回転ラマンスペクトルの間隔を予想せよ。
問題 4.1
以下の振動の、赤外活性・ラマン活性を判別せよ。
a) H2 (伸縮振動)
b) C2H4  1
(全対称 C-H 伸縮)
1
(全対称 C-H 伸縮)
c) N2O [直線N-N-O構造]  2
(変角)
2
(変角)
d) SO2 [三角形]  1
(対称伸縮),
1
(対称伸縮),  3 (反対称伸縮)
3 (反対称伸縮)
問題 4.2
以下の分子の純回転遷移・回転ラマンは活性か、不活性か?
H2, CO2, NH3, SF6
例題 4.3
CH4 赤外  3
バンドの回転線間隔, ~10.0 cm-1, から C-H 結合距離を求めよ
(正四面体を仮定)
3
バンドの回転線間隔, ~10.0 cm-1, から C-H 結合距離を求めよ
(正四面体を仮定)
(4.6) 式 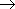 回転線間隔 = 2B.
回転線間隔 = 2B.
よって I = 3.3715 amu 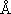 2
[(4.4) 式].
2
[(4.4) 式].
C-H 結合距離を r とすると I = (8/3) 1.0078
r 2 [(4.3) 式].
したがって r = 1.12 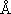 .
.
問題 4.3 CH3 ラジカル (平面三角形構造) の c 軸回転定数, C = 4.742 cm-1, から C-H 結合距離を求めよ。
問題 5.1 Na-D 線遷移の励起状態のスペクトル項を書け。
問題 5.2
水素原子の基底状態のスペクトル項を書け。
また、n = 2 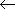 1 遷移
(Lyman-
1 遷移
(Lyman- 線) の励起状態のスペクトル項を書け。
線) の励起状態のスペクトル項を書け。
問題 6.1
1) I2 分子の振動エネルギー準位は 213.76
 - 0.596
- 0.596  2
[cm-1] で表される。
2
[cm-1] で表される。 = 0 の存在比を 1
としたときの、室温 (298 K) における、
= 0 の存在比を 1
としたときの、室温 (298 K) における、 =
1, 2, 3, 4 の準位の存在比を求めよ。
=
1, 2, 3, 4 の準位の存在比を求めよ。
2) 剛体回転子近似のもとに、室温 (298 K) における HI 分子の回転分布
(B = 6.5 cm-1) を求めよ。 (最大値を 1 として存在比が
0.05 以下になるJまで計算せよ)
問題 7.1
O2 分子の基底状態
X 3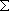 g-
(振動数 1580, B = 1.44 cm-1) と励起状態
A 3
g-
(振動数 1580, B = 1.44 cm-1) と励起状態
A 3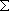 u+
(振動数 799, B = 0.91 cm-1) の 298 K における平衡定数を
(電子励起エネルギーを無視して) 求めよ。
u+
(振動数 799, B = 0.91 cm-1) の 298 K における平衡定数を
(電子励起エネルギーを無視して) 求めよ。
問題 8.1
D2 分子 (2H2H)
の解離平衡定数は同じ温度 (1000, 2000 K) で H2
と、どの程度異なるか?
(調和振動子、剛体回転子を仮定せよ。零点エネルギーの違いは
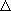 E に反映されることに注意せよ)
E に反映されることに注意せよ)
問題 9.1
1) 反応 Cl + H2 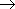 HCl + H
の振動・回転・相対並進・電子状態の 298 K における、
エントロピー変化を以下の情報から計算せよ。
HCl + H
の振動・回転・相対並進・電子状態の 298 K における、
エントロピー変化を以下の情報から計算せよ。
| Cl | H2 | HCl | H | |
振動波数 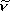 [cm-1]
[cm-1] |
4162 | 2886 | ||
| 回転定数 B [cm-1] | 59.3 | 10.4 | ||
回転対称数 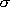 |
2 | 1 | ||
| 質量 m [amu] | 35 | 2 | 36 | 1 |
| 電子状態の多重度 | 4 | 1 | 1 | 2 |
| Cl | H2 | HCl | H | |
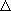 Hf Hf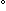 (298 K) [kJ mol-1]
(298 K) [kJ mol-1] |
121.3 | 0 | -92.3 | 218.0 |
問題10.1
以下に示す、水蒸気の蒸気圧における比誘電率
 r の測定値から Debye
式を仮定して、H2O 分子の双極子モーメント
r の測定値から Debye
式を仮定して、H2O 分子の双極子モーメント
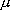 [D] と分極率体積
[D] と分極率体積
 '
[
'
[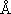 3 = 10-30
m3] を求めよ。
3 = 10-30
m3] を求めよ。
温度 / 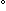 C C |
蒸気圧 / atm |  r r |
| 80 | 0.467 | 1.00305 |
| 100 | 1.000 | 1.00587 |
例題 11.1
[Mn(NCS)6]4- 錯体の Mn
は5つの不対電子をもつ。 磁気モーメントを
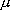 B 単位で予想せよ。
B 単位で予想せよ。
(解) S = (1/2)  5 = 2.5
5 = 2.5
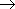
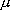 =
2.0023
=
2.0023  (2.5
(2.5 3.5)1/2
3.5)1/2
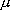 B =
5.92
B =
5.92 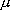 B
B
問題 11.1
気体 O2 は常磁性を示し、 293 K におけるモル磁化率は
4.33  10-8 m3
mol-1 である。 常磁性は主に電子スピンによると仮定して、
気体 O2 のスピン量子数と不対電子数を推定せよ。
10-8 m3
mol-1 である。 常磁性は主に電子スピンによると仮定して、
気体 O2 のスピン量子数と不対電子数を推定せよ。
ただし、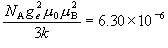 [K m3 mol-1] である。
[K m3 mol-1] である。