2
 g,
2
g,
2 u,
1
u,
1 u,
3
u,
3 g,
1
g,
1 g,
3
g,
3 u
uという説明でしたが、他の講義 (教科書) では、
2
 g,
2
g,
2 u,
3
u,
3 g,
1
g,
1 u,
1
u,
1 g,
3
g,
3 u
uとなっていて、 1
 u と
3
u と
3 g
が入れ替わっています。どちらが本当ですか?
g
が入れ替わっています。どちらが本当ですか?
N2 の分子軌道は、エネルギーの低い方から、
2 g,
2
g,
2 u,
1
u,
1 u,
3
u,
3 g,
1
g,
1 g,
3
g,
3 u
u
という説明でしたが、他の講義 (教科書) では、
2 g,
2
g,
2 u,
3
u,
3 g,
1
g,
1 u,
1
u,
1 g,
3
g,
3 u
u
となっていて、
1 u と
3
u と
3 g
が入れ替わっています。どちらが本当ですか?
g
が入れ替わっています。どちらが本当ですか?
代表的な分子軌道として多くの、物理化学・無機化学・分子軌道法・
化学結合論の教科書に記述があります。大別すると:
(a) E (1 u)
< E (3
u)
< E (3 g)
g)
(b) E (1 u)
~ E (3
u)
~ E (3 g)
g)
(c) E (1 u)
> E (3
u)
> E (3 g)
g)
の3種類の記述があります。
実験的に光電子スペクトルの示す軌道エネルギー順序は (a) であり、
N2+ イオンの電子配置も
1 u4
3
u4
3 g1
であることがわかっています。また最小基底関数系 (Minimal Basis Set)
を用いた分子軌道法の計算 (HF 法) も (a) であることを示します。
このため伝統的には (a) とする解説が多いのですが、
より大きな基底関数系を用いた (より精度が高い) 計算は、わずかに
3
g1
であることがわかっています。また最小基底関数系 (Minimal Basis Set)
を用いた分子軌道法の計算 (HF 法) も (a) であることを示します。
このため伝統的には (a) とする解説が多いのですが、
より大きな基底関数系を用いた (より精度が高い) 計算は、わずかに
3 g
の方がエネルギーが低いことを示しています。光電子スペクトルも厳密には、
N2+ イオンでは
3
g
の方がエネルギーが低いことを示しています。光電子スペクトルも厳密には、
N2+ イオンでは
3 g
から電子が抜けた配置が安定であることを示しているに過ぎないので、中性
N2 分子の分子軌道のエネルギー関係を正確に示すものでは
ありません。したがって、このエネルギー関係は微妙で (b)
のような解説がされることも多くなっています。
(c) のような解説は、等核二原子分子の「わかりやすい」分子軌道として、
2
g
から電子が抜けた配置が安定であることを示しているに過ぎないので、中性
N2 分子の分子軌道のエネルギー関係を正確に示すものでは
ありません。したがって、このエネルギー関係は微妙で (b)
のような解説がされることも多くなっています。
(c) のような解説は、等核二原子分子の「わかりやすい」分子軌道として、
2 g と
3
g と
3 g
の相互作用を無視したものが多いようです。
上の分子軌道法の計算結果から見れば、これも誤りではありません。
g
の相互作用を無視したものが多いようです。
上の分子軌道法の計算結果から見れば、これも誤りではありません。
伝統的な解説に従って (a) と説明していますが、(b) とするのが、正確かもしれません。ここで学ぶべき (教えるべき) 重要なポイントは対称性の同じ分子軌道は相互作用する (混合する) ということですが、N2 分子よりも C2 分子を例にした方がよいのかもしれません。ただ C2 は単離できない不安定分子で、なじみが薄いので N2 を例にとることが多いようです。
N2 の分子軌道において
2 u と
3
u と
3 g
は非結合性軌道という説明でしたが、他の講義 (参考書) では
2
g
は非結合性軌道という説明でしたが、他の講義 (参考書) では
2 u は反結合性、
3
u は反結合性、
3 g は結合性
となっています。どちらが正しいのですか?
g は結合性
となっています。どちらが正しいのですか?
これに関しても、以下の2種類の説明があります。
(a) 2 u - 反結合性,
3
u - 反結合性,
3 g - 結合性
g - 結合性
(b) 2 u - 非結合性,
3
u - 非結合性,
3 g - 非結合性
g - 非結合性
私の講義での説明 (b) は参考書にあげた
「はじめて学ぶ 大学の無機化学」(三吉著、化学同人)
の解説に基づいていますが、(a) のような説明の方が多いようです。
「結合性・反結合性・非結合性」は、
分子軌道や結合次数を理解するために有効な表現ですが、
厳密に定義するのは難しい場合もあります。
分子軌道を構成するもと原子軌道よりもエネルギーが、十分低い=結合性、
あまり変わらない=非結合性、十分高い=反結合性
というのが判定の基準ですが、曖昧な場合は、
それを解釈する人に依存しています。
VB 法的に混成軌道から出発した説明をとると、解釈が変わってくる場合
もあります。
(b) の説明は、O2 と N2
の分子軌道の軌道の違いを示すのによく、またルイス構造や VB
法で出てくる2つの孤立電子対の存在と一致するというメリットが
あるので採用しています。ただし (a) の方が、
 g
(
g
( ) は結合性、
) は結合性、
 u
(
u
( *) は反結合性、
という統一的な説明ができるためわかりやく、一般的だと思います。
*) は反結合性、
という統一的な説明ができるためわかりやく、一般的だと思います。
HF 分子において先生の授業では:
| (a) | 2
| [1s(H)] - 2pz(F) + 2s(F) | 結合性 |
3
| [1s(H)] + 2pz(F) + 2s(F) | 非結合性 | |
1
| 2px(F), 2py(F) (二重縮退) | 非結合性 (lp) | |
4
| 1s(H) + [2pz(F)] + [2s(F)] | 反結合性 | |
| 結合次数 = 1 | |||
| (b) | 2
| 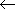 2s(F) 2s(F) | 非結合性 |
3
| 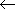 1s(H) と 2pz(F) 1s(H) と 2pz(F)
| 結合性 | |
1
| 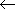 2px(F) or
2py(F) 2px(F) or
2py(F) | 非結合性 | |
4
| 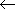 1s(H) と 2pz(F) 1s(H) と 2pz(F)
| 反結合性 | |
| 結合次数 = 1 | |||
これも上の [2] と同様の解釈の違いからくるものです。
私の講義での説明 (a) は参考書にあげた、
(4) 「はじめて学ぶ 大学の無機化学」(三吉著、化学同人)
(5) "Inorganic Chemistry, Third edition," Shriver & Atkins
の解説に基づいています。(4) の参考書には (a), (b)
2つの解釈の両方が示されています。
3 ,
4
,
4 がもっぱら 1s(H) と
2pz(F) からできるという説明 (b) は簡潔でわかりやすいのですが、
実際には 2s(F) の寄与を強く含んでいます。
HF/STO-3G というレベルの量子化学計算における各分子軌道に対する、
原子軌道の寄与を下に示します。
がもっぱら 1s(H) と
2pz(F) からできるという説明 (b) は簡潔でわかりやすいのですが、
実際には 2s(F) の寄与を強く含んでいます。
HF/STO-3G というレベルの量子化学計算における各分子軌道に対する、
原子軌道の寄与を下に示します。
2
| 3
| 1 (x) (x)
| 1 (y) (y)
| 4
| |
| H (1s) | 0.150 | -0.534 | 0 | 0 | 1.054 |
| F (2s) | 0.979 | 0.418 | 0 | 0 | -0.522 |
| F (2px) | 0 | 0 | 1.000 | 0 | 0 |
| F (2py) | 0 | 0 | 0 | 1.000 | 0 |
| F (2pz) | -0.078 | 0.698 | 0 | 0 | 0.816 |
 ,
3
,
3 ,
4
,
4 が H(1s) + F(2s) +
F(2pz) から生成すると考えた場合には、エネルギーの低い方から、
結合性・非結合性・反結合性、となります。
が H(1s) + F(2s) +
F(2pz) から生成すると考えた場合には、エネルギーの低い方から、
結合性・非結合性・反結合性、となります。